โครงการพัฒนา DNA/protein microarray เพื่อใช้ในการตรวจวัดในทางการแพทย์ พัฒนาขึ้นภายใต้แนวคิดการนำความรู้พื้นฐานทางนาโนศาสตร์และนาโนเทคโนโลยีร่วมกับความรู้พื้นฐานการวินิจฉัยโรคมาต่อยอดให้เกิดนวัตกรรม โดยอาศัยเทคโนโลยีการสร้าง microarray ด้วยพอลิเมอร์ไฮโดรเจลร่วมกับการอ่านผลด้วยสมาร์ทโฟน การดำเนินงานวิจัยประกอบด้วย การพัฒนาการเตรียมน้ำหมึกสำหรับพิมพ์ DNA/protein microarray การพัฒนาวิธีการที่ดีที่สุดในการขึ้นรูป DNA/protein microarray การพัฒนาต้นแบบชุดตรวจ alpha-fetoprotein (AFP) สำหรับผู้ป่วยโรคมะเร็ง โครงการจะทำการศึกษาวิจัยและพัฒนา microarray platform ในการตรวจและพัฒนาเทคนิคเพื่อการใช้งาน
Protein และ DNA microarray คือ เทคโนโลยีที่ทำการเตรียม probe molecule หรือโมเลกุลที่จะเป็นตัวจับคู่สารที่ต้องการตรวจวัด เช่น antibody ของเชื้อ หรือ DNA ของสิ่งที่ต้องการตรวจวัด ลงไปบนพื้นผิวพร้อมๆ กันเป็นจำนวนมาก เพื่อใช้ในการตรวจวัดหรือตรวจคัดกรองเชื้อหลายชนิดหรือสายพันธุ์ได้พร้อมๆ กัน ด้วยความก้าวหน้าของเทคโนโลยีการสร้างจุด (spot) ที่สามารถที่จะพิมพ์สารลงไปบนพื้นผิวได้ในปริมาณที่แน่นอน [1] ดังแสดงในรูปที่ 1 นอกจากการเตรียมในลักษณะอาร์เรย์แล้ว ก็ยังสามารถที่จะเตรียมเป็นตัวหนังสือหรือ pattern ตามที่ต้องการ
ความท้าทายของกระบวนการเตรียม protein microarray, DNA microarray หรือ pattern ของ protein/DNA ในการใช้งานจริง คือ การทำให้ spot มีความเสถียร สารกระจายสม่ำเสมอและออกมาให้ความเข้มของแสง fluorescence ที่สม่ำเสมอ และขึ้นตรงกับปริมาณสารที่มีอยู่ กระบวนการที่สารเปียกปอนบนพื้นผิว การแห้งตัว และเกิดเป็น spot นั้นจะเป็นขั้นตอนที่สำคัญในการเตรียม spot เพื่อการใช้งาน การทำความเข้าใจและควบคุมกระบวนการเหล่านี้จึงเป็นเรื่องที่สำคัญ [2] เพื่อไม่ให้เกิดเป็น bad spot เพราะหากมี bad spot เพียงจุดเดียวนั่นหมายถึงความเสียหายที่จะเกิดกับ microarray chip ทั้งแผ่น รูปที่ 2
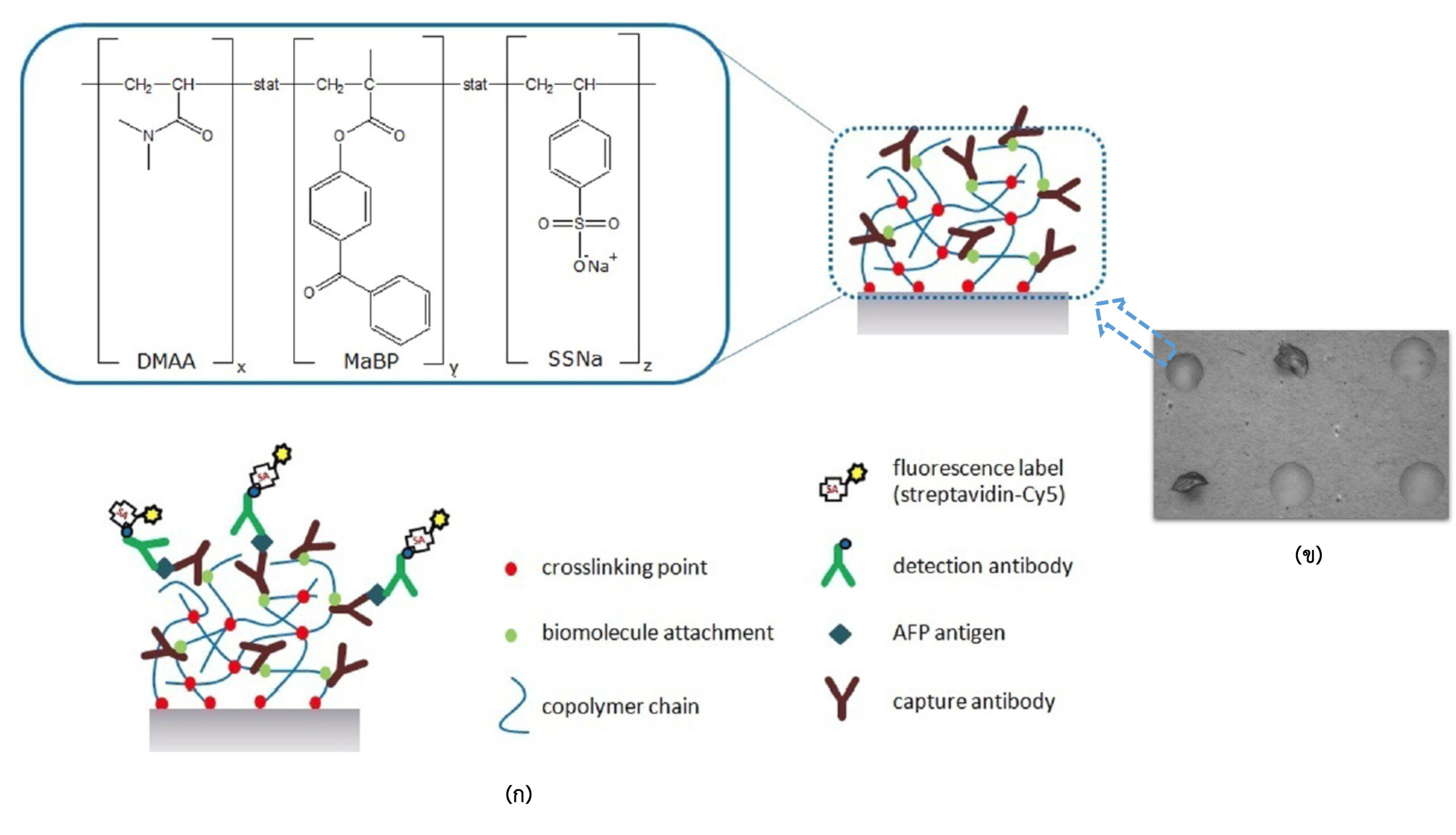
รูปที่ 1 (ก) แสดงการเตรียม protein microarray ของสาร AFP และ (ข) spot ของพอลิเมอร์บนพื้นผิว
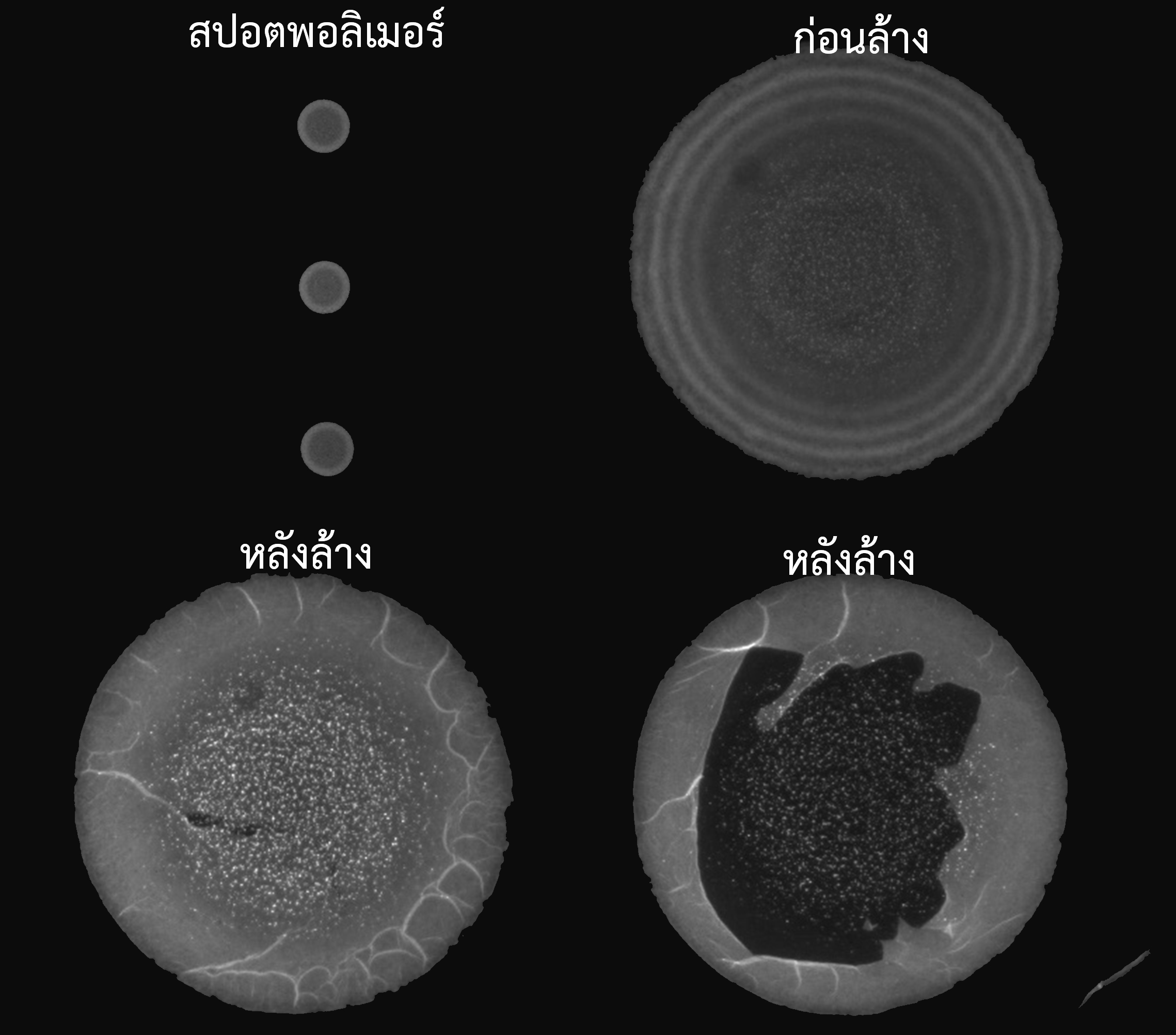
รูปที่ 2 แสดงผลของการเกิด “coffee ring” ที่จะมีผลต่อสัญญาณที่อ่านได้จาก microarray ซึ่งเป็นข้อจำกัดที่สำคัญในการประยุกต์ใช้ Protein microarray, DNA microarray และ Pattern ของ DNA/Protein microarray
ปัจจัยของการเปียกปอน (wettability) และ แรงตึงผิว (surface tension) จะเป็นปัจจัยสำคัญในการควบคุมคุณภาพของจุดที่เตรียมขึ้น ในการศึกษานี้จะประยุกต์ใช้สารประกอบตัวเองชนิดชั้นเดียว (self-assemble monolayer) และ/หรือ พอลิเมอร์ชนิดแปรง (polymer brush) และ/หรือ พอลิเมอร์ไฮโดรเจล (polymer hydrogel) ที่เป็นโครงข่ายใน 3 มิติ มาใช้ในการเตรียม ดังรูปที่ 1 (ก) ซึ่งสารแต่ละตัวก็จะมีสภาวะเหมาะสมที่เฉพาะตัวในการเตรียมสารที่แตกต่างกันไป ในโครงการนี้จะทำการศึกษาและพัฒนาระดับต้นแบบ Protein microarray, DNA microarray และ/หรือ pattern ของ protein/DNA microarray เพื่อการใช้งานในห้องปฏิบัติการในโรงพยาบาล
ระบบที่จะทำการพัฒนา คือ การตรวจวัด AFP ซึ่งเป็น protein ที่ใช้เป็น marker หรือตัวบ่งชี้ในการติดตามการรักษามะเร็ง หรือตรวจเพื่อทำ screening ของมะเร็งตับ [3] และใช้ประกอบการวินิจฉัย down syndrome [4] การตรวจวัดนั้นจำเป็นที่จะต้องใช้ผลการตรวจที่เป็นผลเชิงปริมาณ ซึ่งปัจจุบันใช้เทคนิค ELISA ในการตรวจวัด โรคมะเร็งตับถือได้ว่าเป็นชนิดของมะเร็งที่พบมากเป็นอันดับ 5 ของโลก [5] และเป็นอันดับ 3 ของการทำให้ผู้ป่วยเสียชีวิตได้ [6] สำหรับประเทศไทยนั้นอุบัติการณ์ของโรคมะเร็งตับพบว่ามีอัตรา 40.5 ต่อประชากรชายหนึ่งแสนคน และ 16.3 ต่อประชากรหญิงหนึ่งแสนคน [7] ซึ่งถือว่ามีความอันตรายและอยู่ในอันดับต้นๆ ของระดับความรุนแรงของโรคมะเร็งทั้งหมด มะเร็งเป็นโรคที่ปฏิเสธไม่ได้ว่าหากตรวจพบแล้วหาทางยับยั้งโรคชนิดนี้ได้ยาก ดังนั้นการตรวจพบในระยะเริ่มต้นได้เร็วที่สุดจะเป็นประโยชน์ต่อการรักษาอย่างยิ่ง (early stage prognosis) ตัวบ่งชี้ที่สำคัญในการวินิจฉัยคือ ระดับปริมาณ AFP ที่มีอยู่ในซีรั่มของผู้ป่วย ซึ่ง AFP เป็น tumor marker ที่สำคัญมากในการบอกความผิดปกติของเนื้อร้ายอันก่อให้เกิดโรคมะเร็งตับได้ โดยปัจจุบันการคัดกรองทำได้โดยการวัดปริมาณ AFP ในซีรั่ม และควบคู่กับผลอัลตราซาวน์ ซึ่งปริมาณ AFP ที่พบในคนปกติจะอยู่ในระดับไม่เกิน 20 ng/ml หากพบว่ามีปริมาณ AFP มากกว่า 100 ng/ml มีโอกาสเป็นมะเร็งตับสูง ควรรีบทำการวินิจฉัยอย่างละเอียดโดยแพทย์ผู้เชี่ยวชาญต่อไป [8] จากรายงานการคัดกรองหามะเร็งตับด้วยการตรวจ AFP ควบคู่กับ อัลตราซาวน์ตับ พบว่าสามารถตรวจรักษาในระยะที่สามารถผ่าตัดได้ทัน ซึ่งทำให้ผู้ป่วยมีอัตราการรอดชีวิตได้ดีกว่ากลุ่มที่ไม่ได้ทำการคัดกรอง ดังนั้นสำหรับการตรวจวัดเพื่อประยุกต์ใช้ในงานโรคมะเร็งตับ หากมีการตรวจวัดปริมาณ AFP ในแต่ละช่วง จะเป็นประโยชน์อย่างมาก ทั้งเป็น early detection และติดตามผลกรณีมีความเสี่ยงต่อการเป็นมะเร็งชนิดนี้ จากงานวิจัยก่อนหน้า [1] ได้ศึกษา protein array ของระบบ AFP ทั้งสภาวะการตรึง anti-AFP การเตรียมพื้นผิวที่เหมาะสม และตรวจวัดปริมาณ AFP พบว่า สามารถตรวจวัดปริมาณ AFP ด้วย detection limit 0.01 ng/ml (ในการเตรียมสารตัวอย่างด้วยการเจือจาง 100 เท่า) ดังรูปที่ 1และ 3

รูปที่ 3 แสดงผลปริมาณ AFP ที่ความเข้มข้นต่างๆ ตั้งแต่ 0- 10 ng/ml
จากรายงานวิจัยนี้ จะเป็นประโยชน์กับการตรวจวัดปริมาณ AFP ในซีรั่มที่มีผลของ matrix effect ซึ่งจำเป็นต้องใช้ระบบตรวจวัดที่มี sensitivity สูง และ detection limit ต่ำ ได้เป็นอย่างดี ดังนั้นคณะผู้วิจัยเล็งเห็นความเป็นไปได้ในการนำมาต่อยอดในการประยุกต์กับงานภาคสนามตรวจวัดสารตัวอย่างจริงคือซีรั่มผู้ป่วยในโรงพยาบาลจริง
โครงการจะทำการศึกษาและพัฒนา microarray ร่วมกันของหน่วยย่อยในเครือข่ายระหว่างมหาวิทยาลัยมหิดล มหาวิทยาลัยศรีนครินทรวิโรฒ สถาบันเทคโนโลยีพระจอมเกล้าเจ้าคุณทหารลาดกระบัง และ สถาบันเทคโนโลยีพระจอมเกล้าเจ้าพระนครเหนือ โดยจะดำเนินการพัฒนาร่วมกับหน่วยภูมิคุ้มกันวิทยาและคลินิคัลไมโครสโคปี ภาควิชาพยาธิวิทยา คณะแพทยศาสตร์ โรงพยาบาลรามาธิบดี ในการตรวจและพัฒนาเทคนิคเพื่อการใช้งาน
เอกสารอ้างอิง
- Yodmongkol, B. Sutapun, T. Srikhirin, et al., “Fabrication of protein microarrays for alpha fetoprotein detection by using a rapid photo-immobilization”, Sensing and BioSensing Research 7, 95-999 (2016) 95-99.
- Li, M. Dong, R. Li, L. Zhang, et al., “A fluorometric microarray with ZnO substrate-enhanced fluorescence and suppressed “coffee-ring” effects for fluorescence immunoassays”, Nanoscale 7 (2015) 18453-18458.
- B. Eldad and M. D. Adrian, “Diagnosis of hepatocellular carcinoma”, HPB 7 (2005) 26-34.
- Muller, S. Dreux, J. F. Oury, et al., “Down syndrome maternal serum marker screening after 18 weeks’ gestation”, Prenat. Diagn. 22 (2002) 1001-1004.
- D. Evi and R.D. Joris “Diagnosing and monitoring hepatocellular carcinoma with alpha-fetoprotein: New aspects and applications”, ClinicaChimica Acta 395 (2008) 19-26.
- Liu, X. Li, Z. Zhang, et al., “Nanogram per milliliter‐level immunologic detection of alpha‐fetoprotein with integrated rotating ‐resonance microcantilevers for early‐stage diagnosis of hepatocellular carcinoma”, Biomed Microdevices 11 (2009) 183–191.
- http://www.siamhealth.net/public_html/Disease/cancer/liver_cancer.htm
- Sameer and H. David, “Hepatocellular cancer: A guide for the Internist”, The American Journal of Medicine 120 (2007) 194-202.
รายงานโดย
ผศ. ดร. เติมศักดิ์ ศรีคิรินทร์
ภาควิชาฟิสิกส์และหน่วยสร้างเสริมศักยภาพทางด้านนาโนศาสตร์และนาโนเทคโนโลยี คณะวิทยาศาสตร์ มหาวิทยาลัยมหิดล กรุงเทพมหานคร – 10400
E-mail: toemsak.sri@mahidol.ac.th




