โลหะออกไซด์ (metal oxides) เป็นสารที่ได้รับความสนใจอย่างมากเพื่อนำมาช่วยพัฒนาเทคโนโลยีใหม่ๆ เนื่องจากโลหะออกไซด์มีคุณสมบัติที่หลากหลายไม่ว่าจะเป็น optoelectronic, ferroelectricity, photovoltaic และ photocatalysis นอกจากนี้โลหะออกไซด์บางชนิด อาทิ TiO2 (titanium dioxide), ZnO (zinc oxide) และ SnO2 (tin dioxide) แสดงทั้งคุณสมบัติโปร่งแสงและนำไฟฟ้าได้ดีในเวลาเดียวกัน ทำให้สารเหล่านี้ถูกนำไปใช้ประโยชน์ในด้านต่างๆ เช่น ขั้วไฟฟ้าโปร่งแสง หรือที่เรียกว่า transparent electrodes ที่อยู่ในอุปกรณ์ไฟฟ้าต่างๆ เช่น จอแสดงผล, เซลล์พลังงานแสงอาทิตย์ และ ไดโอดเปล่งแสง รวมถึงนำไปคลือบกระจกที่ทำให้มีคุณลักษณะพิเศษไม่ว่าจะเป็นการกั้นความร้อนม, การกำจัดหมอก และการทำความสะอาดตัวเอง ที่สำคัญในปี พ.ศ. 2515 มีการค้นพบปฏิกิริยาการแยกน้ำโดยใช้แสงบนแผ่นไทเทเนียมไดออกไซด์ (TiO2) ทำให้เกิดแนวความคิดเรื่องการแปลงพลังงานแสงอาทิตย์มาใช้เป็นพลังงานไฟฟ้า และขยายกรอบการศึกษามายังสารโลหะออกไซด์เชิงซ้อนอื่นๆ เช่น SrTiO3 ที่มีช่องว่างระหว่างแถบพลังงานที่กว้างและมีตำแหน่งของแถบพลังงานที่เหมาะสมต่อการนำไปใช้เป็นตัวเร่งปฏิกิริยาแยกน้ำโดยใช้แสงอย่างมาก
การเรียงตัวของอะตอมในผลึกโลหะออกไซด์มักจะมีความบกพร่องเกิดขึ้นเสมอ กรณีที่เข้าใจง่ายที่สุดคือ การที่อะตอมบางตัวภายในผลึกหายไป หรือ การที่อะตอมบางตัวแทรกอยู่ในช่องว่างระหว่างอะตอมอื่น หรือแม้กระทั่งการมีอะตอมอื่นจากภายนอกมาเจือปนอยู่ในผลึก ความบกพร่องนี้เรียกว่าความบกพร่องแบบจุด (point defects) เป็นสิ่งที่ส่งผลกระทบต่อคุณสมบัติเชิงไฟฟ้าและเชิงแสงของผลึกโลหะออกไซด์อย่างมาก ความบกพร่องเหล่านี้อาจเกิดขึ้นได้โดยธรรมชาติหรือเกิดจากเจตนาของผู้ปลูกผลึกก็เป็นได้ ตัวอย่างเช่น ในกระบวนการปลูกผลึก จะมีการปล่อยก๊าซออกซิเจนผ่านโลหะเพื่อรวมเป็นสารประกอบโลหะออกไซด์ ในขณะที่ผลึกเริ่มก่อตัวอะตอมของออกซิเจนหรืออะตอมของโลหะก็ตามอาจไม่เข้าไปอยู่ในตำแหน่งที่ถูกต้อง กล่าวคือในตำแหน่งที่ควรจะมีอะตอมของออกซิเจนอยู่อาจจะไม่มีอะตอมของออกซิเจนก็เป็นได้ เราเรียกว่า oxygen vacancy หรือ ตำแหน่งที่ควรจะมีอะตอมของโลหะอยู่โลหะอาจจะหายไปก็ได้เรียกว่า metal vacancy ซึ่งอะตอมของโลหะหรืออะตอมของออกซิเจนอาจจะเข้าไปแทรกอยู่ระหว่างตำแหน่งอะตอมใดๆ ก็ได้ เรียกว่า interstitial อีกกรณีหนึ่งคือตำแหน่งที่ควรจะมีออกซิเจนอาจจะมีอะตอมโลหะมาแทนที่ได้ ทำนองเดียวกันตำแหน่งที่ควรจะมีโลหะก็อาจจะมีออกซิเจนได้เช่นกันเรียกกรณีนี้ว่า antisites เรียกความบกพร่องเหล่านี้ว่า native defects หรือ intrinsic defects นอกจากนี้อาจจะมีอะตอมจากภายนอกเจือปนเข้ามาในผลึกโดยเกิดขึ้นระหว่างกระบวนสังเคราะห์ผลึกเช่น ไฮโดรเจน(H), ซิลิกอน(Si), ฟลูโอรีน(F), คลอรีน (Cl) และ คาร์บอน (C) เป็นต้น ธาตุเหล่านี้มักจะเข้ามาเจือปนในผลึกโลหะออกไซด์ได้ง่ายแต่ก็ส่งผลต่อประสิทธิภาพของอุปกรณ์ที่ผลิตขึ้นเช่นกัน
สารโลหะออกไซด์นั้นเป็นสารกึ่งตัวนำชนิดเอ็น (n-type) ซึ่งเป็นผลจากการมีความบกพร่องในผลึก ดังนั้นความเข้าใจเชิงลึกของการนำไฟฟ้าที่เกิดขึ้นจากความบกพร่องนี้จะช่วยให้สามารถพัฒนาและปรับปรุงขั้วไฟฟ้าโปร่งแสงที่ผลิตจากโลหะออกไซด์ให้มีประสิทธิภาพดียิ่งขึ้น โดยปกติการนำไฟฟ้านี้เป็นผลมาจากความบกพร่อง 2 ชนิดคือ จากการหายไปของอะตอมของออกซิเจน (oxygen vacancy: VO) และ การที่อะตอมของโลหะไปแทรกตัวระหว่างช่องว่างระหว่างอะตอมอื่นๆ (metal interstitial: Mi) ทั้งสองจะทำหน้าที่เป็นตัวให้อิเล็กตรอน (donor) และมักปรากฏอยู่ในผลึกโลหะออกไซด์ได้ง่าย ในทางทฤษฎีนั้นเราสามารถวิเคราะห์ผลของความบกพร่องต่อคุณสมบัติต่างๆของโลหะออกไซด์ได้โดยวิธีการคำนวณที่เรียกว่าทฤษฎีฟังชันก์นัลของความหนาแน่น (Density-functional Theory: DFT) ทฤษฎีนี้เป็นหนึ่งในวิธีการที่ใช้อธิบายคุณสมบัติของวัสดุต่างๆจากการคำนวณในระดับอะตอม ตัวอย่างที่ผ่านมาจากกลุ่มของเราคือ การศึกษาความบกพร่องในผลึกอินเดียมออกไซด์ (In2O3) [1] ซึ่งเป็นสารกึ่งตัวนำชนิดเอ็นที่นิยมนำมาใช้เป็นสารกึ่งตัวนำแบบใส หากแต่สาเหตุของการนำไฟฟ้านี้ยังเป็นที่ถกเถียงกันอยู่ กลุ่มวิจัยของเราได้ศึกษาความบกพร่องที่เป็นไปได้นั่นคือ การหายไปของอะตอมออกซิเจน (VO) และ อะตอมอินเดียม (VIn), การที่อะตอมแทรกอยู่ระหว่างช่องว่าง (Ini, Oi,) และ การแทนที่ของอะตอม (InO, OIn) เริ่มแรกจะต้องคำนวณหาค่าพลังงานการก่อตัว (formation energy) ของความบกพร่องแต่ละชนิดที่ระดับเฟอร์มี (Fermi level) ต่างๆ ดังรูปที่ 1 โดยค่าพลังงานการก่อเกิดจะสอดคล้องกับความเข้มข้นของความบกพร่องนั้นๆ ผลปรากฏว่า oxygen vacancy (VO) เป็นความบกพร่องที่สามารถเกิดได้ง่ายที่สุดและทำหน้าที่ให้อิเล็กตรอนถึง 2 ตัว เนื่องจากออกซิเจนใน In2O3 ทำพันธะกับอะตอมของอินเดียม 4 ตัว ดังนั้นเมื่ออะตอมออกซิเจนหายไป 1 ตัว จะเกิดอิเล็กตรอนหลุดออกมา 2 ตัว ตามรูปที่ 2
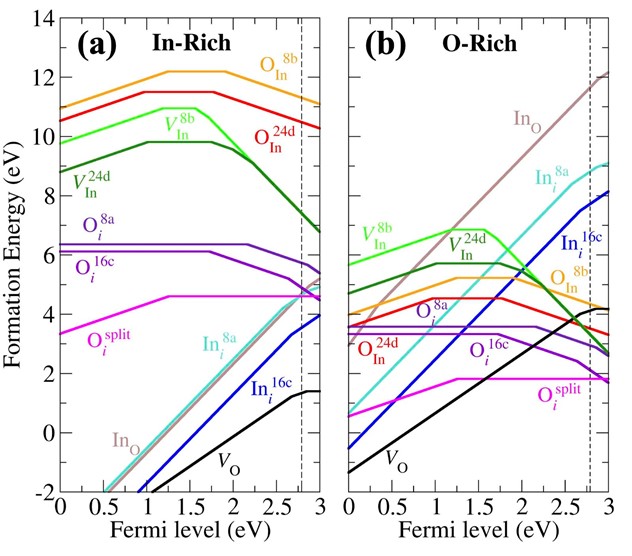
รูปที่ 1 พลังงานการก่อเกิด (Formation energy) ซึ่งเป็นฟังก์ชั่นของระดับพลังงานเฟอร์มีของความบกพร่องแบบจุดชนิดต่างๆ ใน In2O3 ภายใต้เงื่อนไขแบบ (a) In-rich (b) O-rich จุดสูงสุดของแถบฉนวนถูกกำหนดไว้ที่ศูนย์ และเส้นประแสดงจุดต่ำสุดของแถบนำไฟฟ้า
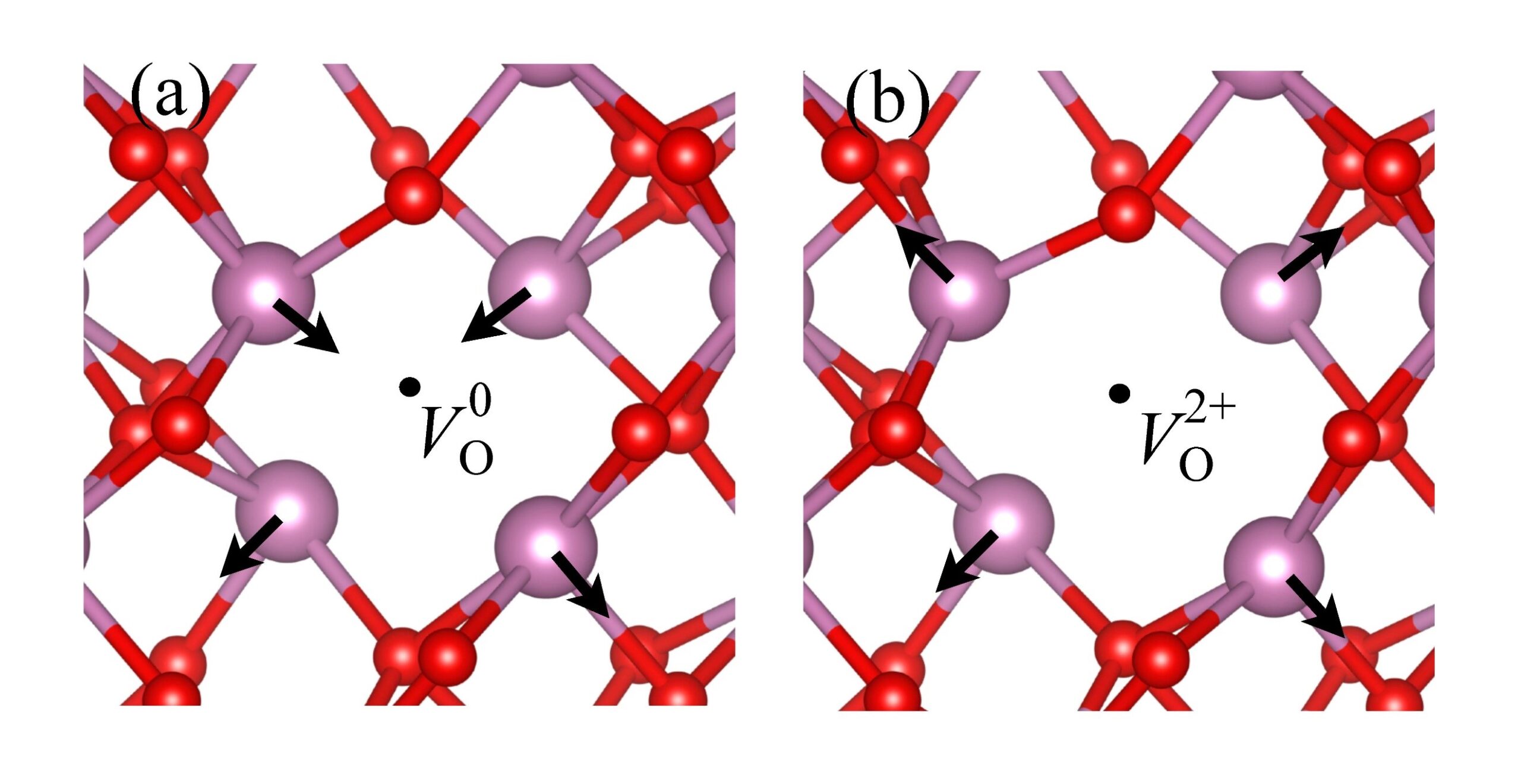
รูปที่ 2 โครงสร้างระดับอะตอมโดยรอบตำแหน่งของ oxygen vacancy ในสถานะประจุ (a) 0 และ (b) 2+
อิเล็กตรอนทั้งสองนี้ต้องการพลังงานเพียงเล็กน้อยที่จะถูกกระตุ้นไปบนแถบนำไฟฟ้าและเกิดการนำไฟฟ้าแบบเอ็นขึ้น จากรูปที่ 1 oxygen vacancy (VO) จะเกิดได้ง่ายเมื่อเราปลูกผลึกที่สภาพแวดล้อมที่ขาดออกซิเจน เรียกว่า O-poor หรือ In-rich ซึ่งจะเกิดขึ้นเมื่อความดันของก๊าซออกซิเจนมีค่าต่ำๆ ในทางตรงกันข้ามหากปลูกผลึกในสภาพแวดล้อมที่มีความดันของก๊าซออกซิเจนมาก (In-poor หรือ O-rich) การที่ออกซิเจนจะหายไปจากผลึกก็เป็นไปได้ยากทำให้ค่าพลังงานงานการก่อตัวมีค่าสูงขึ้น ออกซิเจนที่มีปริมาณมากจะไปแทรกระหว่างอะตอมตัวอื่นๆ เกิดเป็น oxygen interstitial และความบกพร่องที่จะเกิดขึ้นได้อีกก็จะเป็นการหายไปของอะตอมอินเดียม (indium vacancies) นั่นเอง สังเกตได้จากทั้งสองความบกพร่องมีพลังงานต่ำกว่าการหายไปของออกซิเจนเมื่อพลังงานเฟอร์มีอยู่ใกล้แถบนำไฟฟ้า (conduction band) ดังรูปที่ 1 ความบกพร่องสองชนิดนี้ต่างทำหน้าที่เป็นตัวรับอิเล็กตรอน (electron acceptor) ดังนั้นความบกพร่องทั้งสองตัวนี้จะจับอิเล็กตรอนที่เกิดจาก VO ทำให้การนำไฟฟ้าชนิดเอ็น (n-type) ลดลง
นอกเหนือจากความบกพร่องตามธรรมชาติแล้ว เราสามารถเจือธาตุอื่น ๆ เข้าไปในผลึกออกไซด์ได้เช่นกัน วัตถุประสงค์ของการเจือนี้ก็เพื่อปรับปรุงและพัฒนาโลหะออกไซด์ให้มีคุณสมบัติตามความต้องการที่จะนำไปใช้ ตัวอย่างที่เห็นได้ชัดก็คือการเจืออะตอมจำพวกแอนไอออน(anion) เข้าไปในผลึกของ TiO2 และ SrTiO3 เพื่อเพิ่มความสามารถในการดูดกลืนแสงจากดวงอาทิตย์โดยเพิ่มการดูดกลืนแสงในช่วงที่ตามองเห็น ปกติแล้วการดูดกลืนแสงจะเกิดขึ้นจากการกระตุ้นอิเล็กตรอนจากแถบฉนวน (valence band) ไปแถบนำไฟฟ้า (conduction band) โดยจะต้องใช้พลังงานอย่างน้อยเท่ากับขนาดของช่องว่างระหว่างแถบทั้งสองนี้ แต่เนื่องจากผลึกโลหะออกไซด์มีช่องว่างระหว่างแถบพลังงานที่กว้าง ทำให้การดูดกลืนแสงเกิดขึ้นในช่วงอัลตราไวโอเลต(UV) เท่านั้น เมื่อนักทดลองเจือไนโตรเจนเข้าไปในผลึกของ SrTiO3 เขาพบว่าปฏิกิริยาที่ถูกกระตุ้นด้วยแสงมีประสิทธิภาพดีมากยิ่งขึ้น เพราะการดูดกลืนพลังงานสามารถเกิดได้ในช่วงที่ตามองเห็นได้ กลไกที่เกิดขึ้นเป็นเรื่องที่ถกเถียงกันอย่างมาก กลุ่มวิจัยของเราได้ทำการอธิบายสิ่งที่เกิดขึ้นจากการคำนวณโดยใช้ฟังก์ชันนัลแบบลูกผสม (hybrid functional) [2] จากการศึกษาพบว่าไนโตรเจนที่เจืออยู่ในผลึกสามารถอยู่ได้ในหลากหลายรูปแบบทั้งเข้าไปแทนที่อะตอมออกซิเจนโดยตรง (NO) และ ความบกพร่องเชิงซ้อนอื่น ๆ คือ (NO)O, (NO2)2O, (N2)O และ split-interstitial (N2)2O ดังรูปที่ 3 แต่รูปแบบที่เสถียรที่สุดคือการที่ไนโตรเจนไปแทนที่ออกซิเจนโดยตรง เมื่อผลึกเป็นสารกึ่งตัวนำชนิดเอ็นภายใต้เงื่อนไขแบบ O-poor, O-rich และเงื่อนไขระหว่างกลาง ความบกพร่องลักษณะนี้ทำให้เกิดแถบพลังงานใหม่ในช่องหว่างระหว่างแถบฉนวนและแถบนำไฟฟ้าและเกิดเป็นกระบวนการ จากการคำนวณพบว่าการดูดกลืนนี้เกิดขึ้นได้ตั้งแต่ย่านแสงที่ตามองเห็นนั่นเอง (แสดงในรูปที่ 4) นอกจากนี้เรายังพิจารณาผลของความบกพร่องจากไฮโดรเจนซึ่งเกิดขึ้นได้ง่ายระหว่างกระบวนการปลูกผลึกด้วย จากการคำนวณพบว่าอะตอมไฮโดรเจนจะทำพันธะกับอะตอมไนโตรเจน เกิดเป็นความบกพร่องเชิงซ้อน NO-Hi และทำให้พลังงานดูดกลืนมีค่ามากขึ้นเล็กน้อย ต่างจากเหตุการณ์เดียวกันใน TiO2 ที่การเกิดความบกพร่องเชิงซ้อน NO-Hi ทำให้การดูดกลืนแสงในช่วงที่ตามองเห็นหายไป นอกจากนี้เรายังพบว่า (NO2)2O และ (N2)O ทำให้ SrTiO3 สามารถดูดกลืนแสงในย่านที่ตามองเห็นด้วยเช่นกัน สุดท้ายเราคำนวณค่าความถี่ของการสั่นของพันธะที่เกิดจากความบกพร่องของไนโตรเจนเพื่อให้นักทดลองสามารถนำค่านี้ไปใช้ในการระบุชนิดของความบกพร่องที่เกิดขึ้นได้
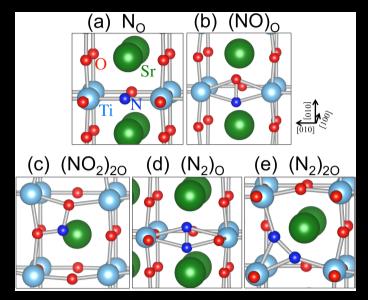
รูปที่ 3 โครงสร้างระดับอะตอมของความบกพร่องชนิดต่างๆที่เกิดจากไนโตรเจนใน SrTiO3 : (a) NO, (b) (NO)O, (c) (NO2)2O, (d) (N2)O, and (e) (N2)2O
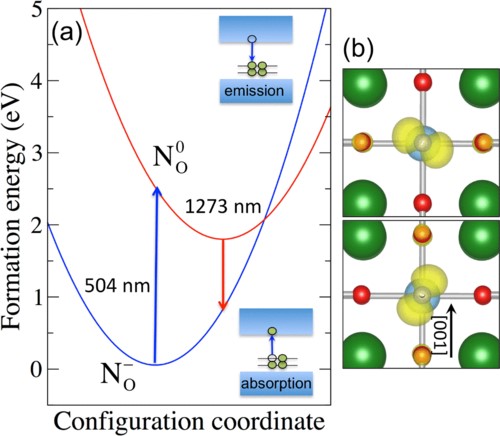
รูปที่ 4 (a) แผนภาพ configuration coordinate สำหรับ NO (b) ความหนาแน่นประจุของสถานะ 2p จาก NO ที่สอดคล้องกับกระบวนการดูดกลืนแสง
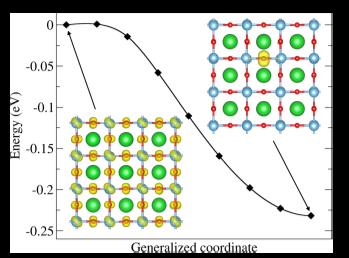
เมื่อไม่นานมานี้กลุ่มวิจัยของเราได้ศึกษาอีกประเด็นของความบกพร่องในรูปแบบที่เรียกว่าโพลารอนขนาดเล็ก (small polaron) ซึ่งเกิดจากการกักตัวเองของโฮลใน BaTiO3 [3] ผลการคำนวนแสดงให้เห็นว่าโฮลใน BaTiO3 มักจะอยู่ในรูปของการกักตัวเอง หรือ self-trapping มากกว่าการกระจายตัวอยู่ทั่วผลึก BaTiO3 (แสดงในรูปที่ 5) นอกจากนี้การกักตัวเองของโฮลใน BaTiO3 ยังเสถียรมากกว่าการกักตัวเองของโฮลใน SrTiO3 และยังพบได้ง่ายที่อุณหภูมิสูงๆอีกด้วย ยิ่งไปกว่านั้นเราได้คำนวณการปลดปล่อยพลังงานแสงที่เกิดจากกระบวนการรวมตัวของอิเล็กตรอนจากแถบนำไฟฟ้าและโฮลที่ถูกกักตัวนี้ด้วย พบว่าพลังงานแสงที่ปลดปล่อยมีค่า 2.17 eV สุดท้ายนี้เราพิจารณาการเคลื่อนที่ของโฮลที่ถูกกักตัวเองและเปรียบเทียบกับผลที่ได้จากการทดลองด้วย
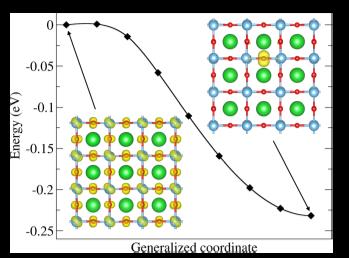
รูปที่ 5 แผนภาพ Configuration coordinate สำหรับการแปลงจากสถานะ delocalize hole ใน BaTiO3
ความบกพร่องและสิ่งเจือปนต่างๆรวมถึงโพลารอนขนาดเล็กในผลึกโลหะออกไซด์ล้วนแต่ส่งผลต่อคุณสมบัติเชิงไฟฟ้าและเชิงแสงของวัสดุทั้งสิ้น โดยทำให้เกิดแถบพลังงานแถบใหม่ขึ้นในช่องหว่างระหว่างแถบฉนวนและแถบนำไฟฟ้า และนำไปสู่การให้อิเล็กตรอนและโฮลในแถบนำไฟฟ้าและแถบฉนวน แม้ว่าความบกพร่องในผลึกจะหลีกเลี่ยงได้ยากแต่เราก็สามารถควบคุมการเกิดความบกพร่องต่างๆ ระหว่างการปลูกผลึกได้ ส่วนการเจืออะตอมภายนอกเข้าไปเป็นการกระทำเพื่อต้องการพัฒนาคุณสมบัติของผลึก ปัจจุบันมีการเจืออะตอมต่างๆ ในผลึกโลหะออกไซด์เพื่อปรับปรุงประสิทธิภาพของผลึกเมื่อนำไปใช้ ตลอดจนขยายขอบเขตการใช้ประโยชน์อีกด้วย ตัวอย่างหนึ่งที่ยังเป็นประเด็นที่น่าสนใจคือการเจือให้โลหะออกไซด์เป็นทั้งสารกึ่งตัวนำชนิดเอ็นและชนิดพี ซึ่งเราแทบจะไม่สามารถทำได้เพราะลักษณะพิเศษของโครงสร้างทางไฟฟ้าของโลหะออกไซด์และตำแหน่งของแถบฉนวนที่อยู่ต่ำมากจึงไม่เอื้อต่อการเกิดปริมาณโฮลที่มากพอ ทำให้การนำโลหะออกไซด์ไปใช้ประโยชน์จึงถูกจำกัด ประเด็นนี้จึงเป็นอีกเรื่องสำคัญที่นักวิทยาศาสตร์พยายามที่จะศึกษาหาทางสร้างและพัฒนาสารกึ่งตัวนำชนิดพีจากโลหะออกไซด์ต่อไป
เอกสารอ้างอิง
- Chatratin, I., Sabino, F.P., Reunchan, P., Limpijumnong, S., Varley, J.B., Van de Walle, C.G. and Janotti, A., 2019. “Role of point defects in the electrical and optical properties of In2O3” . Physical Review Materials, 3(7), p. 074604.
- Reunchan, P., Umezawa, N., Janotti, A., Jiraroj, T. and Limpijumnong, S., 2017. “Energetics and optical properties of nitrogen impurities in SrTiO3from hybrid density-functional calculations”. Physical Review B, 95(20), p. 205204.
- Traiwattanapong, W., Janotti, A., Umezawa, N., Limpijumnong, S., T-Thienprasert, J. and Reunchan, P., 2018. “Self-trapped holes in BaTiO3”. Journal of Applied Physics, 124(8), p. 085703.
รายงานโดย
รศ. ดร. สิริโชค จึงถาวรรณ
สาขาวิชาฟิสิกส์ สำนักวิทยาศาสตร์ มหาวิทยาลัยเทคโนโลยีสุรนารี จ. นครราชสีมา – 30000
E-mail: sirichok@sut.ac.th”